MISS. LIC. LIRA NÉLIDA SALOMÉ MONTERO -PRIMER GRADO - AULA No 2
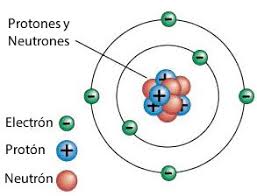
1. EL ÁTOMO.- Parte más pequeña de una sustancia que no se puede descomponer químicamente. Cada átomo tiene un núcleo (centro) compuesto de protones (partículas positivas) y neutrones (partículas sin carga). Los electrones (partículas negativas) se mueven alrededor del núcleo. Los átomos de diferentes elementos contienen diferentes números de protones, neutrones y electrones.
2. MODELOS ATÓMICOS:
Este modelo esta formado por un NUCLEO ATÓMICO donde se encuentran dos partículas sub-atómicas los PROTONES Y LOS NEUTRONES.
- LA ENVOLTURA ELECTRÓNICA .-Esta formada por 7 NIVELES DE ENERGÍA :
K - L - M - N - O - P - Q o también enumerados 1 ,2,3,4,5,6,7 donde se encuentran girando los ELECTRONES. ( e-)
K - L - M - N - O - P - Q o también enumerados 1 ,2,3,4,5,6,7 donde se encuentran girando los ELECTRONES. ( e-)
CARACTERÍSTICAS INHERENTES AL NÚCLEO DEL ÁTOMO:
Las características inherentes al núcleo del átomo son:
a. EL NUMERO ÁTÓMICO.
b. EL NUMERO DE MASA O PESO ATÓMICO
C. EL NÚMERO DE NEUTRONES.
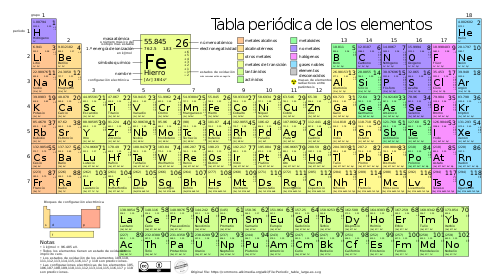
A. EL NÚMERO ATÓMICO:_ Se le representa con la letra Z, este número lo encontraras en la tabla periódica de los elementos químicos, este número nos indica el número de electrones ( e-) , el número de protones (p+) , y el lugar que ocupa el elemento químico en la tabla periódica. por ejemplo:
1.Hallar el Z de Litio: Z= 3 esto significa que el átomo de Litio tiene 3 electrones, tiene 3 protones y ocupa el lugar No 3 en la T.P.
2. Hallar el Z de Calcio: Z= 20 , esto significa que el átomo de calcio tiene 20 electrones, tiene 20 protones y ocupa el lugar No 20 en la T.P
Hallar: Z de HIDRÓGENO
Hallar: Z del ALUMINIO
Hallar: Z de ZINC
B. NÚMERO DE NEUTRONES: (No)
El número de Neutrones nos da a conocer cuantos neutrones hay o existen en el núcleo del átomo. Si quieres calcular cuántos neutrones tiene un átomo, solo tienes que restar el número de protones, o número atómico, del número de masa.
Entonces la fórmula seria: No = A - Z
Entonces podemos decir que EL NÚMERO DE NEUTRONES ES IGUAL NÚMERO DE MASA MENOS EL NÚMERO ATÓMICO
Ejemplo: HALLAR EL NÚMERO DE NEUTRONES DEL ÁTOMO DE MERCURIO
Aplicamos la fórmula ; No = A- Z
No = A - Z
No = 200,59 - 80
No = 201 - 80
No = 121
HALLAR EL NÚMERO DE NEUTRONES DEL ÁTOMO DE NITRÓGENO.
HALLAR EL NÚMERO DE NEUTRONES DEL ÁTOMO DE ZINC
HALLAR EL NÚMERO DE NEUTRONES DEL 'ATOMO DE CARBONO.
C. EL NÚMERO DE MASA O PESO ATÓMICO:
El número másico (A) indica la masa total del átomo (tomando en cuenta que los electrones no aportan una masa significativa, se puede tomar como que es la masa del núcleo).El número de masa se encuentra en la tabla Periódica de los elementos químicos.
pero también se puede hallar aplicando la siguiente fórmula:
A = Z + N
ó A = P+ + N
Entonces sabiendo estos datos podemos afirmar que EL NÚMERO DE MASA SERA IGUAL AL NÚMERO DE PROTONES MAS EL NÚMERO DE NEUTRONES.
HALLAR EL NÚMERO DE MASA ( A ) DEL ÁTOMO DE L CLORO:
Aplica la fórmula:
A = P+ + No
A = 17 + 18
A = 35
CARACTERÍSTICAS INHERENTES A LA ENVOLTURA ELECTRÓNICA.
1. En la envoltura electrónica llamado también nube electrónica se encuentran girando los electrones en los Niveles de Energía u orbitales.
2. LOS NIVELES DE ENERGÍA SON SIETE: K - L - M - N - O - P - Q
3. Dentro de los NIVELES DE ENERGÍA también se encuentran los SUB-NIVELES DE ENERGÍA denominados con las las letras minúsculas : s , p , d , f estas letras provienen de las siguientes palabras .
S = Sharp
P = Principal
D = Difusa
F = Fundamental
Cada uno de estos sub - niveles contiene un número determinado de orbitales designados con las letras : x, y, z
REGLAS DE DISTRIBUCIÓN ELECTRÓNICA:
1. Los niveles de energía son 7, se encuentran en la envoltura del átomo: K -L-M-N-O-P-Q
2. Cada nivel de energía contiene una determinada cantidad de electrones, así tenemos:
1k = 2e-
2L = 8e-
3M= 18e-
4N = 32e-
5O = 32e-
6P = 18e-
7Q = 8e-
2. Cada nivel de energía presenta un número determinado de sub-niveles de energía, estos subniveles son : s, p, d, f
S = 2e-
P = 4e-
d = 10e-
f = 14e-
Niveles de Energía: Sub-niveles de energía: No de e-
1K s = 2e- 2e-
2L s = 2e- , p = 6e- 8e-
3M s = 2e- , p = 6e- , d= 10e- 18e- 4N s = 2e- , p = 6e- , d = 10e-, f= 14e- 32e-
5O s = 2e- , p = 6e- , d = 10e-, f= 14e- 32e- 6P s = 2e- , p= 6e- , d = 10e- 18e-
7Q s = 2e-, p = 6e- 8e-
Ejemplos de distribución electrónica:
Realiza la distribución electrónica del átomo de litio Li=
Se puede escribir de manera Horizontal esta regla , claro y se vería de la siguiente forma:
1s2, 2s2, 2p4, 3s2 , 3p4, 4s2, 3d10, 4p4, 5s2 , 4d10, 5p4,6s2 , 4f14
1. Realiza la distribución electrónica del átomo de Berilio (Be)
Nota importante : Para realizar la distribución electrónica de los átomos de los elementos químicos es muy necesario conocer y tener en cuenta el Número atómico del elemento químico. ( Z).
ejemplo:
-EL Número Atómico del Berilio es 4, esto significa que el berilio tiene 4 electrones, y su distribución seria de la siguiente manera:
Be = 1s2, 2s2
Realizar la distribución electrónica de los siguientes átomos:
carbono Z= 6e-
oxígeno Z= 8e-
hidrógeno Z= 1e-
calcio Z= 20e-
La unión de los átomos forman las moléculas o compuestos químicos, estos átomos para unirse, implican a sus electrones a los últimos electrones que tienen en el último nivel de energía, ahí según se realice la unión, estos átomos ganan pierden o comparten electrones , estos átomos se unen a través de enlaces, enlaces químicos
-enlace covalente.
-enlace electrovalente.
-enlace metálico.
ESTIMADOS ESTUDIANTES, GRACIAS, CUIDENSE Y MUCHAS BENDICIONES PARA TODOS
LOS QUIERO.













No hay comentarios.:
Publicar un comentario